Medizinische Projekte
240.000 € der Deutschen Forschungsgemeinschaft (DFG) für Forschungsprojekt zum Rhabdomyosarkom
 Mit Unterstützung der Kinderkrebshilfe Münster e.V. erforscht Dr. Dr. Sebastian Balbach seit einigen Jahren Mechanismen der Genregulation beim Rhabdomyosarkom, einem bösartigen Muskeltumor. Die Kinderkrebshilfe Münster e.V. unterstützte die Forschungsgruppe nicht nur mit einer Start-Up-Hilfe bei der Grundausstattung mit Reagenzien, sondern verstärkte auch mit Finanzspritzen die Frauenpower (Elina Richter, studentische Hilfskraft, Vertragsverlängerung von Eva Kremer, Doktorandin).
Mit Unterstützung der Kinderkrebshilfe Münster e.V. erforscht Dr. Dr. Sebastian Balbach seit einigen Jahren Mechanismen der Genregulation beim Rhabdomyosarkom, einem bösartigen Muskeltumor. Die Kinderkrebshilfe Münster e.V. unterstützte die Forschungsgruppe nicht nur mit einer Start-Up-Hilfe bei der Grundausstattung mit Reagenzien, sondern verstärkte auch mit Finanzspritzen die Frauenpower (Elina Richter, studentische Hilfskraft, Vertragsverlängerung von Eva Kremer, Doktorandin).
Das Team um den Assistenzarzt der Klinik für Pädiatrische Hämatologie und Onkologie am Universitätsklinikum Münster (UKM) untersucht, wie Krebszellen mRNA, also die Montageanleitungen für Proteine, herstellen. Viele Krebszellen sind dabei auf mRNAs angewiesen, die für gesunde Zellen verzichtbar sind. Dr. Balbach konnte zeigen, dass Rhabdomyosarkomzellen absterben, wenn das Spleißen, ein wichtiger Schritt der mRNA-Produktion in den Tumorzellen, gestört wird, weil für Tumorzellen essentielle mRNAs nicht mehr produziert werden können.
Die Erfolge dieser Arbeiten haben nun auch die Deutschen Forschungsgemeinschaft (DFG) überzeugt, das Projekt für zwei Jahre mit knapp 240.000 € zu fördern. Das DFG-Projekt soll klären, wie genau Substanzen wirken, die das Spleißen blockieren, und ob sie zukünftig zur Therapie von Rhabdomyosarkomen und anderen Krebserkrankungen im Kindes- und Jugendalter eingesetzt werden könnten.
Die leukämische Stammzelle – Ein vielversprechender Ansatz in der Krebsforschung
 Mit den modernen Methoden der Kinderkrebsbehandlung können heute mehr als 85% der an einer Leukämie erkrankten Kinder und Jugendlichen geheilt werden. Trotzdem wird es weiter Kinder geben, denen mit der herkömmlichen Chemotherapie nicht geholfen werden kann, oder bei denen die Leukämie nach Jahren erneut wieder ausbricht (Rezidiv).
Mit den modernen Methoden der Kinderkrebsbehandlung können heute mehr als 85% der an einer Leukämie erkrankten Kinder und Jugendlichen geheilt werden. Trotzdem wird es weiter Kinder geben, denen mit der herkömmlichen Chemotherapie nicht geholfen werden kann, oder bei denen die Leukämie nach Jahren erneut wieder ausbricht (Rezidiv).
Ein Bericht von Dr. med Sebastian Balbach
Eine Erklärung liefert die Stammzellforschung: Die Leukämie geht von Krebsstammzellen aus, die aus Vorläuferzellen der Blutbildung entstehen. Die genetische Information unserer Zellen ist ständiger Schädigung durch Strahlung, Infektionen oder Giftstoffe ausgesetzt. Meist werden diese Mutationen sofort repariert, oder sie sind ungefährlich, weil sie unwichtige Stellen betreffen. Werden aber Gene zerstört, die z.B. einer unkontrollierten Zellteilung Einhalt gebieten, oder Gene aktiviert, die Zellen zur Vermehrung anregen, kann eine Zelle ihre ursprüngliche Funktion vergessen und zu einer Tumorstammzelle werden (Entdifferenzierung). Im Gegensatz zu den meisten anderen Körperzellen können Stammzellen sich unbegrenzt vermehren. Aus einigen Stammzellen entstehen dann über schnell teilende Vorläuferzellen die eigentlichen Tumorzellen. Die meiste Zeit jedoch ruhen Stammzellen. Das macht sie unerreichbar für die herkömmliche Chemotherapie, die hauptsächlich schnell teilende Zellen angreift.
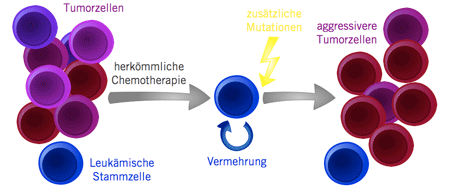
Durch die Chemotherapie wird die Zahl der Leukämiezellen sehr effektiv reduziert. Kaum ist ein Therapiezyklus jedoch beendet, teilen sich die Stammzellen wieder und produzieren neue Leukämiezellen. Die Therapie der Leukämie umfasst deswegen sehr viele Zyklen, um die immer wiederkehrenden Leukämiezellen zu vernichten. Meist gelingt es so, die Stammzellen aus der Reserve zu locken und ebenfalls abzutöten. Im Lauf der Erkrankung kann die Stammzelle jedoch durch weitere Mutationen noch resistenter gegen Chemotherapie werden. Irgendwann kann dann eine zurückgebliebene Stammzelle zu einem schwer zu behandelndem Rezidiv führen.
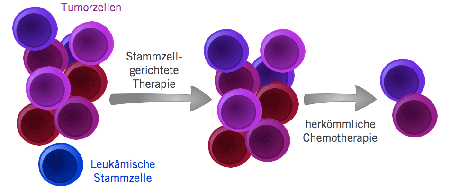
Ziel aktueller Forschung ist daher eine Stammzell-gerichtete Therapie, die zunächst die leukämischen Stammzellen vernichtet. Die eigentlichen Leukämiezellen könnten dann durch eine kurze herkömmliche Chemotherapie zerstört werden.
Ansätze gibt es viele: Eine spezifische Immuntherapie verwendet Antikörper, die gezielt an die Stammzellen binden und diese für das Immunsystem zum Abschuss freigeben oder Medikamente überbringen. Hierfür müssen möglichst alle Tumorstammzellen, aber möglichst wenige gesunde Körperzellen mit dem Antikörper markiert werden. Ein zweiter Ansatz ist die gezielte Blockade der Stammzell-Neubildung, um den Nachschub an Tumorstammzellen zu unterbrechen. In klinischer Erprobung sind bereits Wirkstoffe, die Stammzellen aus ihrem Rückzugsbereich vertreiben und sie so für herkömmliche Chemotherapie angreifbar machen sollen. Außerdem wollen Forscher die Entdifferenzierung rückgängig machen, durch die aus einer gewöhnlichen Körperzelle eine Tumorstammzelle geworden ist.
 Voraussetzung für die Entwicklung zielgerichteter Therapien ist die genaue Kenntnis der Tumorstammzellen; ihre Isolierung und genaue Charakterisierung ist daher ebenfalls Gegenstand aktueller Forschung auf diesem vielversprechenden Gebiet. Hier setzt auch ein neues Forschungsprojekt der Abteilung für pädiatrische Hämatologie und Onkologie der Uniklinik Münster an, das von der Kinderkrebshilfe Münster e.V. unterstützt wird.
Voraussetzung für die Entwicklung zielgerichteter Therapien ist die genaue Kenntnis der Tumorstammzellen; ihre Isolierung und genaue Charakterisierung ist daher ebenfalls Gegenstand aktueller Forschung auf diesem vielversprechenden Gebiet. Hier setzt auch ein neues Forschungsprojekt der Abteilung für pädiatrische Hämatologie und Onkologie der Uniklinik Münster an, das von der Kinderkrebshilfe Münster e.V. unterstützt wird.







